생체 대사 과정들이 빠르게 진행될 수 있도록 물질대사 속도를 높일 매개자가 필요함
1. 촉매
반응을 매개한 후 그 자신은 아무런 화학적 변화를 일으키지 않는 물질
반을 시 생성 물질의 양 변화 없이 오직 활성화 에너지만 바꿔 반응의 속도를 변화시킴
| 근접성 | 반응물들 사이에 충돌 횟수를 증가시킴 (압력↑. 부피↓ 시 더 효과가 큼) |
| 방향성 | 반응물들의 충돌 시 화학 반을을 잘 일으킬 수 있도록 충돌 방향을 잡아줌 |
| 활성화 에너지 | 더 많은 분자가 활성화 에너지 장벽을 넘게 해 유효 충돌 횟수를 늘려줌 |
| 온도 | 보통 무기 촉매들이 관여하는 반응의 경우 온도가 상승하면 반응 속도도 증가함 |
2. 효소
생체 내에서 일어나는 여러 가지 화학반응의 촉매 역할을 수행하는 단백질
(i) 구조
단순 단백질 효소 : 단백질로만 이루어진 효소(대다수의 가수분해 효소들)
복합 단백질 효소 : 전효소 = 주효소(단백질) + 보조인자(비단백 물질)
보조인자가 주효소와 비공유 결합을 한 경우 : 조효소 (coenzyme)
보조인자가 주효소와 공유결합을 한 경우 : 보결 분자단 ( Prosthetic group)
효소의 기질 결합 부위를 이루는 아미노산들의 R기와 기질 분자 사이에 수소 결합, 이온 결합, 소수성 결합, 반 데르 발스 결합, 공유 결합 등을 형성해 반응을 일으킴
(ii) 작용 방식
ㄱ) 근접성과 방향성
기질들의 충돌 횟수를 증가시키고 기질 분자들의 방향을 잡아서 반응이 잘 일어나도록 함
ㄴ) 비용 매화(Desolvation)
기질을 감싸고 있는 물 분자를 떼어내서 반응을 일으키는 작용기들을 노출시킴
ㄷ) 기질 특이성
기질 결합 부의(active site)의 자리들이 기질을 삼차원적으로 인식하면서 기질 결합 부위와 정확하게 들어맞는 기질과만 반응을 함
ㄹ) 활성화 에너지
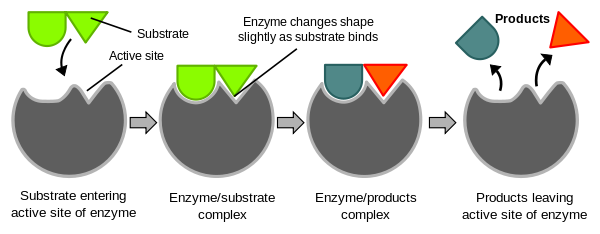
유도 적합설(induced-fit)
효소와 기질이 결합하는 과정에서 효소의 기질 결합 부위의 모양에 가벼운 변화가 일어나 기질과 잘 들어맞게 됨
ㅁ) 전이 상태 인식(Transition state)
기질 결합 부위의 구조가 기질과 산물의 중간 단계인 전이 상태의 물질과 잘 들어맞는 모양을 취함
기질이 들어올 때 효소의 기질 결합 부위 내 여러 R기들과 다양한 상호 작용을 통해 기질의 모양이 전이 상태로 쉽게 바뀌게 되어 산물의 생성 속도가 빨라짐
(iii) 성질
주로 단백질로 이루어져 있어서 온도와 pH에 민감함(단백질 3차 구조의 변성 요인들)
반응을 매개한 후 그 자신은 아무런 화학적 변화를 일으키지 않음
3. 리보자임(Ribozyme)
RNA가 생체 내의 일부 반응들의 촉매 역할을 함